Физическая химия
Значение курса физической химии состоит также в том, что этот курс создает своеобразный мост между экологическими задачами и соответствующими научными принципами и инженерным, аппаратурным оформлением соответствующего оборудования, аппаратов, приборов, технических конструкций. Понятно, что решение этой проблемы требует не только знания принципов и положений физической химии, но и соответствующих практических навыков выполнения необходимых расчетов, технических разработок, инженерных чертежей (в том числе, с использованием современной компьютерной техники).
Понятно, что владение положениями физической химии важно не только собственно для профессиональной подготовки будущих специалистов - экологов, но и в более широком смысле - для расширения научного и технического кругозора студентов, повышение общего уровня их экологической культуры.
Это должно способствовать решению важной проблемы природоохранной деятельности по улучшению экологического состояния окружающей среды, очистки воздуха, повышение качества питьевой воды, почвы, пищевых продуктов.
Курс физической химии играет также немаловажную роль в индивидуальной работе с талантливыми студентами подготовка студенческих научных публикаций и докладов на областные, всеукраинские и международные научные конференции, конкурсных студенческих научных работ, подготовка студентов к участию в первом и втором турах Всеукраинских олимпиад по химии, экологии, безопасности жизнедеятельности.
Понятие физическая химия возникло еще в XVII в., А получило распространение только в XVIII в. В первой половине XVIII в. появился советчик под названием «Физическая химия», в котором приводились физико-химические описания явлений, происходящих вокруг нас. Химия воспринималась как искусство разделять вещества на составные части (анализ) и складывать тела из них источников (синтез). Но все это не имело никакого отношения к науке.
Основная задача ученых на то время было превратить химию из искусства в науку. Утверждению идеала физики, которая уже тогда была самостоятельной наукой благодаря работам Исаака Ньютона, в химии заметно способствовали работы Н.В. Ломоносова, который отмечал перспективе полезного взаимосвязи химии и физики: «Обе науки, - утверждал он, - благодаря взаимной помощи получают мощное развитие, так легче распознать скрытую природу тел, если мы соединим физические истины с химическими».
М.В. Ломоносову принадлежит первая программа физико-химических исследований. Центральное место в пои встает количественным измерениям: «Проверить все, что только можно измерять, взвешивать и определять вычислениями». Чтобы понять это высказывание ученого, стоит обратить внимание на то, что раньше все химико - аналитические описания явлений сводились к качественному анализу. То утверждали, что данное вещество тверже или мягче, чем другая, длинная, или шире. Неумение количественно описать то или иное явление приводило химиков к неверным выводам, вследствие чего невозможно установить какие-то закономерности в химии. Например, вес веществ считалась их качество и, как и любая качество, она должна была зависеть во температуры, давления и других факторов. Качественно это подтверждалось и в опытах, поскольку нагрева некоторых материалов влекло или уменьшения их веса (за счет десорбции газов, например), или повышение (за счет окисления).
Поэтому становится понятным, почему все опыты М.В. Ломоносова в 1752 - 1756 годах были направлены на «измерения меры, веса и их пропорций». Пройдет много времени и Д.И. Менделеев скажет: «В природе мера и вес - главное оружие познания». Таким образом, работы М.В. Ломоносова и параллельно английского ученого Дж. Блока утверждали основополагающий принцип сохранения массы веществ в химических реакциях. Тогда же было высказано мнение, что атомы веществ имеют достаточно определенную массу. Это дало возможность Дж. Дальтону в 1803 г. открыть один из важнейших законе »химии - закон простых кратных отношений, который с помощью представлений об атомах позволил объяснить причину определенных отношений элементов в химических соединениях. Таким путем сформировалось атомное учение - химическая атомистика, которая определила развитие химии в Вельможа времени.
В дальнейшем (XIX-XX вв.) Физическая химия трудами Д.У. Гиббса. Д.И. Менделеева, Вант-Гоффа, В.Ф. Оствальда, Св. Аррениуса, А.Л. Ле Шателье, В. Нернста и др.. сформировалась в гак называемую классическую физическую химию, которая включала в себя: термохимии, электрохимии, фазовые равновесия, учение о растворах и химическую кинетику.
Обновление классической физической химии состоялось в начале XX ст. Особенно чувствовалась в ней на ту нору недостаток четкой и физически обоснованной теории строения атомов и химической связи. Все это она потом получила от физики, которая создала квантовую теорию строения атома и образования химической связи. Современная физическая химия включает в себя также учение о строении атомов и молекул, природу химической связи и химическую кинетику.
Физическая химия - это самостоятельная наука, изучающая взаимосвязь физических и химических явлений. Главная задача физической химии - предусмотреть прохождение химического процесса во времени и конечный результат (состояние равновесия) при различных условиях па основе данных о строении и свойствах молекул веществ, создающих систему. Иными словами, физическая химия - это наука, которая использует законы физики для объяснения химических явлений. Термин «физическая химия» и определение этой науки, как уже отмечалось, были впервые предложены М.В. Ломоносовым в 1752-1754 годах: «Физическая химия - это наука, которая па основе положений и опытов физики объясняет, то, что происходит в смешанных телах при химических реакциях». Признание физической химии как самостоятельной науки и учебной дисциплины произошло в утверждении в Лейпцигском университете 1887 первой кафедры физической химии во главе с выдающимся химиком В.Н. Оствальдом.
Различают физическую и химическую форму движения материи. Для химической, т.е. химического процесса, характерно изменение числа и расположения атомов в молекулах веществ, реагирующих между собой. А это, в свою очередь, зависит от физической формы движения - колебания атомов и молекул.
Физическая химия делится па классическую и современную. Классическая физическая химия состоит из следующих разделов:
1. Химическая термодинамика, изучающая фундаментальные соотношения, основываются на I и II законах термодинамики. Эти соотношения позволяют: рассчитать количество тепла, поглощаемого или выделяется в любом процессе, определить возможность самопроизвольного протекания процесса в желаемом направлении, определить условия равновесия и направление смещения процесса при изменении внешних условий.
2. Термодинамика растворов, которая изучает их природу, внутреннюю структуру и важнейшие пласты посту. Последние рассматриваются в функциональной зависимости от концентрации и химической природы компонентов.
3. Физико-химический анализ гетерогенных систем, где рассматриваются вопросы фазовых равновесий одно-, двух-, трехкомпонентных систем, их фазовые диаграммы и методы их исследования.
4. Электрохимия, которая изучает взаимосвязь между преобразованиями химической энергии па электрическую, свойства растворов электролитов, их электропроводность, явление электролиза, работу гальванических элементов и электрохимическую коррозию металлов.
5. Химическая кинетика и катализ - это определение скоростей и механизма химических реакций, а также явления катализа.
В современной физической химии прилагаются разделы о строении вещества, где изучается связь между строением атомов и молекул и их физическими и химическими свойствами, и фотохимия - наука о химичци реакции под действием света.
Как определил выдающийся современный физико-химик Н.Н. Эммануэль, есть три главные составляющие химии Вельможа времени: химическая статика, изучающая состав и строение веществ, химическая динамика, которая имеет дело с механизмами и законами превращений веществ, и, наконец, химические явления, открытия и использования которых во многом определяют успехи современного научно-технического прогресса (высокотемпературная сверхпроводимость, полупроводниковая техника, термоядерный синтез и т.д.).
 Рассмотрим общие условия равновесия гетерогенной системы, состоящей из р фаз и к компонентам.
Рассмотрим общие условия равновесия гетерогенной системы, состоящей из р фаз и к компонентам.
Подробнее: Общие условия равновесия в гетерогенных системах. Правило фаз Гиббса
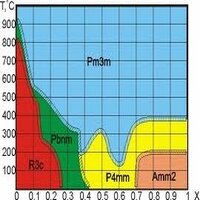 Гетерогенными называются системы, которые в разных частях имеют разные физико-химические свойства.
Гетерогенными называются системы, которые в разных частях имеют разные физико-химические свойства.
Подробнее: Применение второго закона термодинамики к фазовых превращений
 1. Охарактеризуйте становления физической химии как самостоятельной науки. Предмет и задачи дисциплины. Основные разделы классической физической химии.
1. Охарактеризуйте становления физической химии как самостоятельной науки. Предмет и задачи дисциплины. Основные разделы классической физической химии.
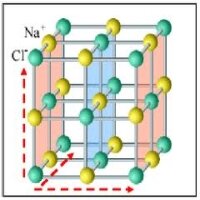 Интегрируя изобары или изохоры химической реакции, невозможно получить выражение
Интегрируя изобары или изохоры химической реакции, невозможно получить выражение
 Во время химической реакции через некоторое время устанавливается состояние равновесия
Во время химической реакции через некоторое время устанавливается состояние равновесия
 Важным свойством закрыто системы является ее способность выполнять работу.
Важным свойством закрыто системы является ее способность выполнять работу.
 Второй закон термодинамики не является абсолютным законом природы (как периной закон)
Второй закон термодинамики не является абсолютным законом природы (как периной закон)
Подробнее: Статистический характер второго закона термодинамики
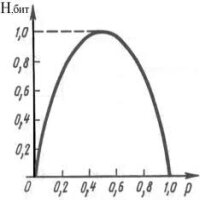 Пусть пространство сосуда разделены значком па две равные части
Пусть пространство сосуда разделены значком па две равные части
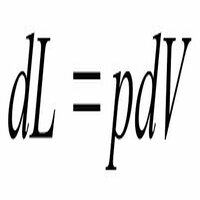 Первый закон термодинамики характеризует энергетические балансы и позволяет вычислить тепловые эффекты химических реакций при стандартных условиях (закон Гесса) и при любой температуре (закон Кирхгоффа).
Первый закон термодинамики характеризует энергетические балансы и позволяет вычислить тепловые эффекты химических реакций при стандартных условиях (закон Гесса) и при любой температуре (закон Кирхгоффа).
 Одной из важнейших тепловых характеристик веществ и процессов в экосистемах является теплоемкость.
Одной из важнейших тепловых характеристик веществ и процессов в экосистемах является теплоемкость.