Химия
 В молекуле незамещенного бензола электронная плотность распределена равномерно, поэтому электрофильный реагент может атаковать в равной степени любой из шести атомов углерода.
В молекуле незамещенного бензола электронная плотность распределена равномерно, поэтому электрофильный реагент может атаковать в равной степени любой из шести атомов углерода.
 1. Окисление бензольного цикла. Бензольное кольцо устойчиво к действию окислителей. В обычных условиях ни перманганат калия, ни азотная кислота, ни оксил хрома (VI), ни другие сильные окислители не окисляют бензол.
1. Окисление бензольного цикла. Бензольное кольцо устойчиво к действию окислителей. В обычных условиях ни перманганат калия, ни азотная кислота, ни оксил хрома (VI), ни другие сильные окислители не окисляют бензол.
 Реакции присоединения не характерны для аренов, они протекают в жестких условиях.
Реакции присоединения не характерны для аренов, они протекают в жестких условиях.
1.Гидрирование. При повышенных температуре и давлении, в присутствии катализаторов (мелкопористый никель — никель Ренея) бензол и всю гомологи присоединяют три молекулы водорода.
 При атаке электрофильной частицей л-электронной системы бензольного кольца п результате электростатического взаимодействуя образуется неустойчивый л-комплекс. Далее электрофил «вырывает» пару электронов из ароматического секстета бензольного ядра и между ним и одним из атомов углерода образуется о-связь.
При атаке электрофильной частицей л-электронной системы бензольного кольца п результате электростатического взаимодействуя образуется неустойчивый л-комплекс. Далее электрофил «вырывает» пару электронов из ароматического секстета бензольного ядра и между ним и одним из атомов углерода образуется о-связь.
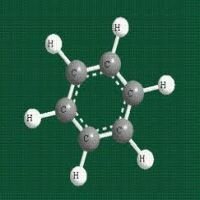 Бензол и его низшие гомологи представляют собой жидкости, обладающие специфическим запахом. Ароматические углеводороды не растворимы в воде и хорошо растворяются в органических растворителях.
Бензол и его низшие гомологи представляют собой жидкости, обладающие специфическим запахом. Ароматические углеводороды не растворимы в воде и хорошо растворяются в органических растворителях.
Подробнее: Физические свойства и химические свойства ароматических углеводов
 По заместительной номенклатуре ИЮПАК одноядерные арены рассматривают как производные бензола. При наличии в кольце двух и более заместителей их положение указывают цифрами.
По заместительной номенклатуре ИЮПАК одноядерные арены рассматривают как производные бензола. При наличии в кольце двух и более заместителей их положение указывают цифрами.
 Простейшим представителем одноядерных ароматических соединений является бензол (С(Н6).
Простейшим представителем одноядерных ароматических соединений является бензол (С(Н6).
Впервые бензол был получен английским ученым М. Фарадеем в 1825 г. из светильного газа, образующегося в процессе переработки каменного угля.
 Ароматическими первоначально называли органические соединения, которые или сами имели приятный запах, или же выделялись из природных веществ, обладающих приятным запахом.
Ароматическими первоначально называли органические соединения, которые или сами имели приятный запах, или же выделялись из природных веществ, обладающих приятным запахом.
 Алкины, подобно алкенам, подвергаются окислению по месту тройной связи. Продуктами реакции являются соответствующие карбоновые кислоты. В качестве окислителей используют перманганат калия в нейтральной или щелочной среде, озон и др.
Алкины, подобно алкенам, подвергаются окислению по месту тройной связи. Продуктами реакции являются соответствующие карбоновые кислоты. В качестве окислителей используют перманганат калия в нейтральной или щелочной среде, озон и др.
 Образование ацетиленидов. Способность ацетиленов с концевой тройной связью отдавать протон позволяет говорить о них как о соединениях, проявляющих кислотные свойства.
Образование ацетиленидов. Способность ацетиленов с концевой тройной связью отдавать протон позволяет говорить о них как о соединениях, проявляющих кислотные свойства.